Фибробласты. Восстановление кожи
В этой статье поговорим о функции дермальных фибробластов в коже, процессе их старения, а также о методе обновления и стимуляции регенерации кожи путём введения аутологичных фибробластов.
Введение
Роль дермальных фибробластов (ДФ) в обновлении кожи трудно переоценить, поскольку они являются основным клеточным компонентом соединительнотканной основы кожи, обеспечивающим её гомеостаз и морфофункциональную организацию. Очевидна актуальность этой темы для регенеративной (репаративной) косметологии, задача которой — омоложение кожи путём активации естественных процессов её восстановления.
Функции дермальных фибробластов
Из всех функций ДФ наибольшее внимание специалистов в области эстетической медицины и дерматологии сосредоточено на продуцировании этими клетками компонентов внеклеточного матрикса (ВКМ) дермы: коллагена, эластина, протеогликанов, особенно гиалуроновой кислоты (ГК), и структурных гликопротеинов.
Повышенный интерес именно к этой функции ДФ понятен: названные компоненты ВКМ формируют и поддерживают структуру кожи, обеспечивая её упругость и прочность. Причём ДФ не только синтезируют эти вещества, но и обеспечивают их катаболизм путём прямого фагоцитоза «отработанных» фрагментов фибрилл коллагена и эластина, секреции коллагеназы, гиалуронидазы и прочих ферментов.
Резидентные клетки ткани — образующиеся и постоянно пребывающие в этой ткани.
Другая, и не менее значимая для кожи, активность ДФ оставалась до недавнего времени несколько на обочине поля зрения врачей-практиков, однако сегодня она тоже становится объектом пристального внимания клиницистов. Речь идёт о целом ряде важнейших функций фибробластов. Так, продуцируя коллаген IV типа и ламинин, они влияют на формирование базальной мембраны. Фибробласты формируют строму, которая не только служит каркасом (опорой) для эпителия, но и регулирует структурную организацию и функционирование эпителиальных клеток. Они вырабатывают и выделяют факторы клеточного роста (KGF-1 — фактор роста кератиноцитов, GM–CSF — гранулоцитарно-макрафагальный колониестимулирующий фактор роста), иммунорегуляторные интерлейкины IL-6, IL-8. За счёт секреции факторов роста и интерлейкинов и непосредственного взаимодействия с эпителиальными клетками ДФ играют ключевую роль в регуляции эпидермального морфогенеза. Их паракринная активность служит основой для поддержания гомеостаза стволовых кератиноцитов.
Дермальные фибробласты секретируют факторы, влияющие на дифференцировку лимфоцитов, и факторы, регулирующие численность, миграцию и функции гранулоцитов и макрофагов, обеспечивая тем самым поддержание иммунитета кожи. Вырабатывая множество проангиогенных факторов, которые индуцируют дифференцировку и миграцию эндотелиальных клеток, ДФ способствуют образованию и стабилизации сосудов.
Они принимают участие в процессах нейроэндокринной регуляции кожи. Синтезируют биологически активные пептиды: гормоны, биогенные амины, нейропептиды и нейротрансмиттеры, идентичные таковым в центральной нервной и эндокринной системах, экспрессируют рецепторы андрогенов и эстрогенов, посредством которых осуществляется влияние этих гормонов на кожу человека.
Фибробласты, взаимодействуя с различными резидентными клетками: эпидермальными, эндотелиальными, нервными, жировыми, гемопоэтическими, участвуют практически во всех кожных процессах, в том числе — физиопатологических. Таким образом, ДФ представляют собой центральное звено в биологии кожи: они поддерживают не только гомеостаз ВКМ дермы, обеспечивая её ремоделирование и обновление, но и физиологическое состояние других слоёв и структур кожи.
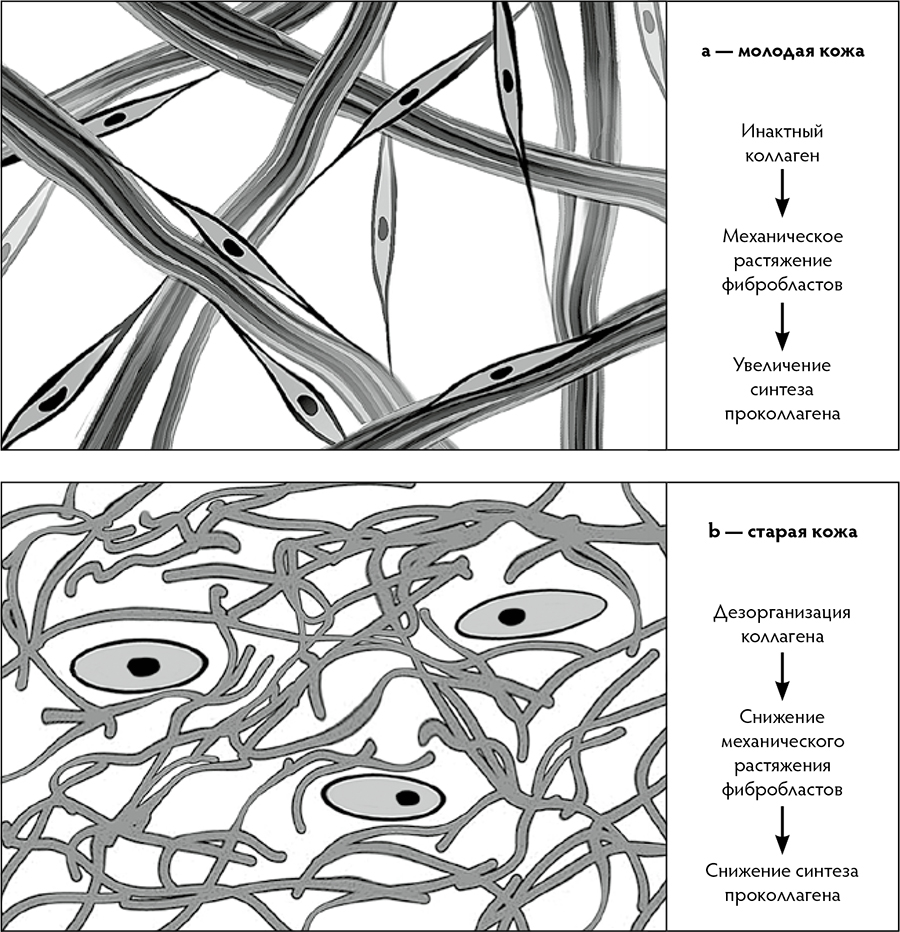
Инволюция дермальных фибробластов
По мере старения организма растёт число ДФ, в которых происходят возрастзависимые изменения, связанные преимущественно с непрерывным накоплением повреждений. Такие ДФ обозначают как «стареющие», или сенесцентные фибробласты (ДФст). Снижается их способность к ремоделированию и организации ВКМ, так как уменьшается синтез и секреция ими основных компонентов ВКМ. Нарушается эпидермальный гомеостаз из‑за негативных изменений в паракринных механизмах, связывающих эпидермис и папиллярный слой дермы. В популяции ДФст происходит увеличение секреции богатого цистеином ангиогенного индуктора — белка 61 (CYR61, или CCN1), стимулирующего продукцию провоспалительных цитокинов и матриксных металлопротеиназ (MMPs). CCN1 и MMPs поддерживают старение клетки путём негативной регуляции гомеостаза коллагена и увеличения его деградации.
Постепенно баланс между синтезом и деградацией коллагена нарушается в пользу последней. Повреждённый коллагеновый каркас ВКМ уже не может удерживать фибробласты в растянутом состоянии, свойственном молодым клеткам. Происходит своего рода коллапс фибробластов, что приводит к нарушению их функций. В процессе инволюции уменьшается численность фибробластов. Снижается и биосинтетическая активность этих клеток, нарушается баланс между синтезом и деградацией ВКМ дермы. В среднем, у пожилых / старых людей, по сравнению с молодыми, общее количество ДФ меньше на 35 %, продукция коллагена в коже снижена на 75 %, причём содержание коллагена уменьшается приблизительно на 1 % в год.
Все сенесцентные изменения в популяции ДФ приводят к постепенному и значительному снижению способности кожи к регенерации и обновлению. Как при этом меняется статус кожи? Уменьшается её толщина, снижается упругость и эластичность, появляются морщины, заломы, птоз тканей — кожа стареет.
Очевидно, что именно ДФ должны быть основной «мишенью» омолаживающих кожу косметологических методов. Так оно и есть: все современные терапевтические воздействия в целях коррекции возрастных изменений кожи — инъекционные, включая PRP-терапию, аппаратные (лазерные, радиочастотные, ультразвуковые) — направлены прежде всего на стимуляцию функциональной активности ДФ, как пролиферативной, так и биосинтетической. Особое место в этом ряду занимает применение аутологичных (собственных) дермальных фибробластов, или SPRS-терапия.
SPRS-терапия как метод оздоровления и обновления кожи
SPRS-терапия (SPRS — от англ. Service for Personal Regeneration of Skin — персонифицированный комплекс лечебно-диагностических процедур для восстановления кожи) — метод регенеративной медицины (РУ ФС №2009 / 308 от 21.07.2010). Его применение позволяет восполнить уменьшившуюся с возрастом популяцию ДФ за счёт введенных в кожу специализированных молодых и функционально активных клеток. Трансплантируются собственные фибробласты кожи пациента, поэтому они полноценно приживаются, интегрируют с резидентной клеточной популяцией и живут «по законам» дермы.
После трансплантации их биосинтетическая активность сохраняется не менее года, причём без какой‑либо дополнительной стимуляции. Как результат, увеличивается синтез коллагена и других компонентов ВКМ, благодаря чему происходит ремоделирование микроструктуры дермы, увеличение её толщины, уменьшение количества и глубины морщин.
Сенесценция — это состояние, при котором клетки с накопленными повреждениями ДНК и истощением механизмов её восстановления перестают делиться, теряют способность к ремоделированию и организации ВКМ.
Описание технологии
В специализированной лаборатории Института стволовых клеток человека, соответствующей международным стандартам GMP*, из 4 мм биоптата кожи пациента получают клеточный препарат, содержащий культивированные аутологичные ДФ (аутоДФ). На этапах клеточного процессинга происходит отбор и стимуляция только функционально активных ДФ, которые, несмотря на старение организма, сохраняют высокую способность к делению и синтезу важных для кожи компонентов. Дело в том, что пролиферативный потенциал всей популяции дермальных фибробластов взрослого человека в течение всей его жизни остаётся на довольно высоком уровне — благодаря наличию в фибробластическом диффероне стволовых / прогениторных клеток. Это клетки-предшественницы, которые отвечают за обновление клеточной популяции дермы. Как показали исследования in vitro, первичные культуры, полученные даже от очень пожилых людей (95 лет), содержат до 14 % митотически активных фибробластов.
Данный факт подтверждается и нашими экспериментами: культуры фибробластов дермы, полученные от пациентов 18–82 лет, характеризуются довольно высокой эффективностью колониеобразования (45.0±9.5 %), независимо от возраста донора. Это даёт возможность из небольшого биоптата кожи любого взрослого человека получить необходимое для проведения терапии количество функционально активных клеток.
После трансплантации культивированных ауто ДФ в дерму их биосинтетическая активность сохраняется. В своей работе мы вводили полученный клеточный материал одновременно и в кожу лица, и в кожу за ушной раковиной, откуда затем проводили забор биоптата для гистологического изучения. Наши исследования показали:
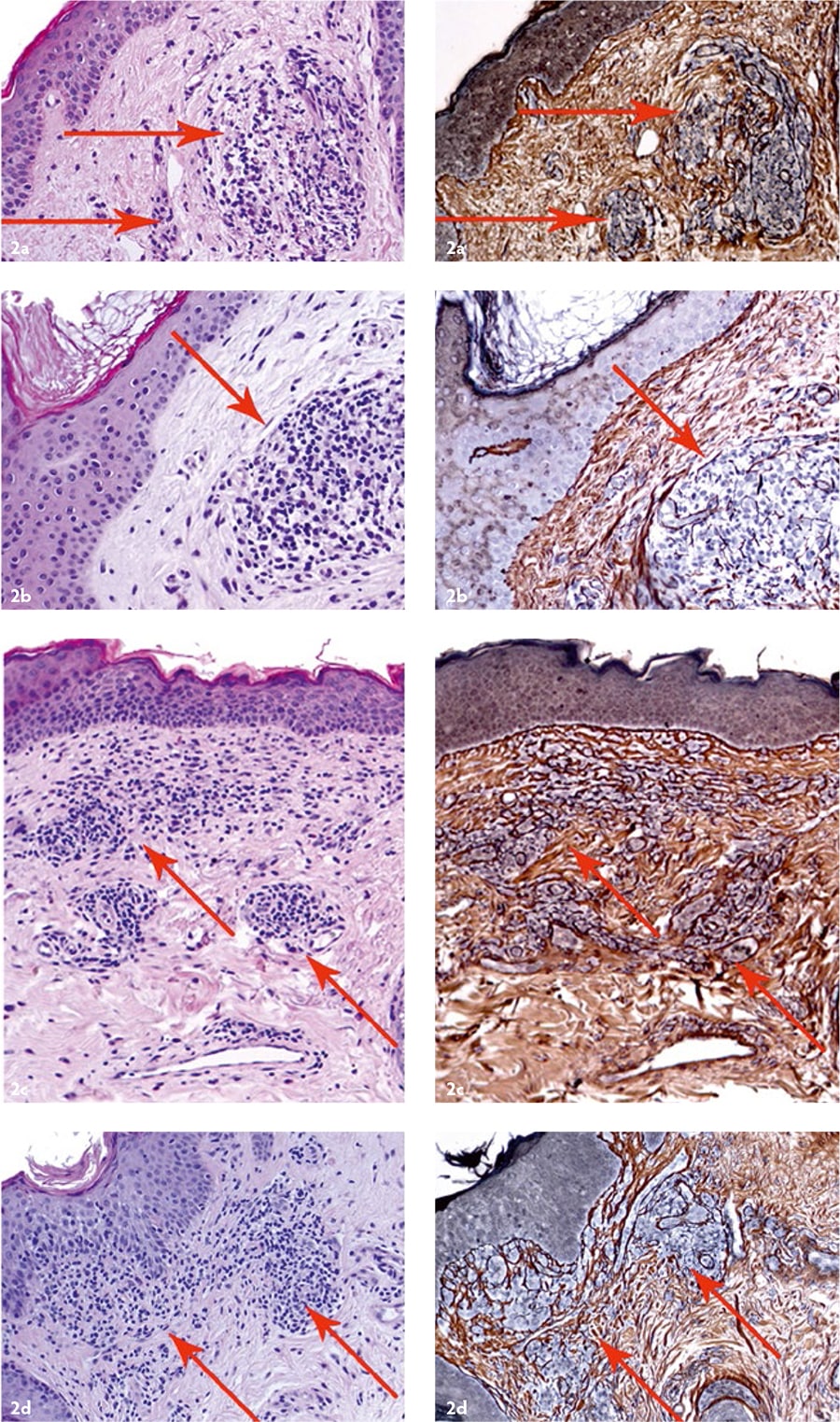
- трансплантированные аутоДФ синтезировали компоненты ВКМ дермы на протяжении как минимум 12 месяцев [Рис. 2];
- трансплантированные аутоДФ присутствовали в дерме небольшими группами, без признаков митотической активности, то есть без признаков деления клеток (следовательно, риск развития каких‑либо гиперпластических процессов при их использовании отсутствует);
- образовались новые коллагеновые волокна;
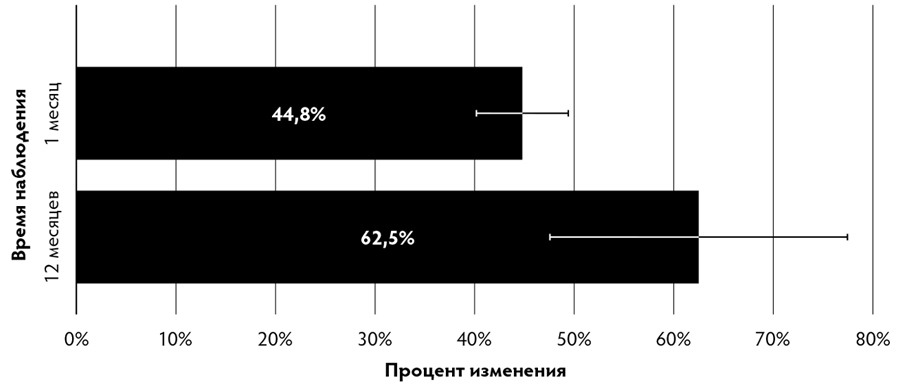
- толщина дермы увеличилась в среднем на 62,5±13,6 % (р=0,028) в течение первых 12 месяцев после применения аутоДФ [Рис. 3].
Через 24 месяца после применения аутоДФ в дерме также регистрировали отдельные группы фибробластоподобных клеток [Рис. 4], продуцирующих коллагеновые волокна. Однако признаков созревания (утолщения) коллагена не наблюдали, из чего следует, что через два года после трансплантации аутоДФ интенсивность их синтетической активности (по сравнению с таковой в течение первого года после трансплантации) была снижена.
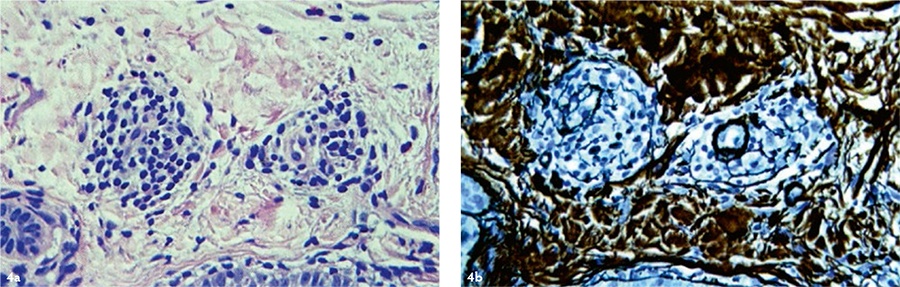
Скорее всего, это связано с уровнем физиологических потребностей дермы (известно, что для обеспечения её физиологического состояния достаточно незначительной функциональной активности фибробластов). По всей видимости, трансплантированные аутоДФ полноценно интегрировались с дермой, стали естественной составляющей её основной клеточной популяции — фибробластического дифферона — и находятся под контролем микроокружения.
Выводы гистологического исследования:
- введенные аутоДФ сохраняют свою жизнеспособность в дерме;
- они располагаются в дерме преимущественно группами;
- их функционирование не приводит к неблагоприятным последствиям, клетки пролиферативно не активны;
- на всех сроках наблюдения в дерме регистрируются признаки увеличения её объёма и процесс синтеза молодых коллагеновых волокон.
Выявленная на гистологическом уровне положительная динамика изменений кожи после применения аутоДФ полностью соответствует клинической картине. Уже через 10–14 дней после окончания курса SPRS-терапии отмечается повышение упругости кожи, уменьшение её рельефности (уменьшение выраженности морщин), улучшение цвета и контуров лица. Эффект имеет нарастающий характер. Так, если через месяц после инъекции на «хорошо» и «отлично» клинический результат оценили 88 % пациентов, то уже через три месяца и позже — 100 %. Врачи-исследователи через месяц определили результат как «хороший» и «отличный» у 86 % пациентов, через три месяца и позже — у 100 % пациентов. Положительные, прогрессирующие со временем (на протяжении как минимум 12 месяцев) изменения состояния кожи подтверждены нами и с помощью инструментальных методов исследования.
Заключение
Инновационная технология — SPRS-терапия, основанная на принципах регенеративной медицины, — позволяет восстанавливать утраченные с возрастом структуру и функции дермы за счёт уникального биологического механизма собственных коллагенобразующих клеток кожи пациента.
SPRS-терапия используется в отечественной эстетической медицине более восьми лет, зафиксировано более 1000 клинических наблюдений пациентов, из которых более 80 % повторно (два и более раз), пролечив одну область кожи, обращались в клиники для лечения этим методом кожи других областей.
Для врачебной практики важно, что SPRS-терапия является не только самостоятельным эффективным методом ремоделирования дермы, но и хорошей базовой основой для применения других косметологических вмешательств, направленных на стимуляцию синтетической активности фибробластов, что позволяет в течение длительного времени поддерживать кожу пациента в хорошем состоянии.
Авторы:
Алла Зорина, к. м. н., врач-биохимик, Москва.
Вадим Зорин, к. б. н., врач-биофизик, Москва.
Журнал: Облик. Esthetic guide №6(29)
